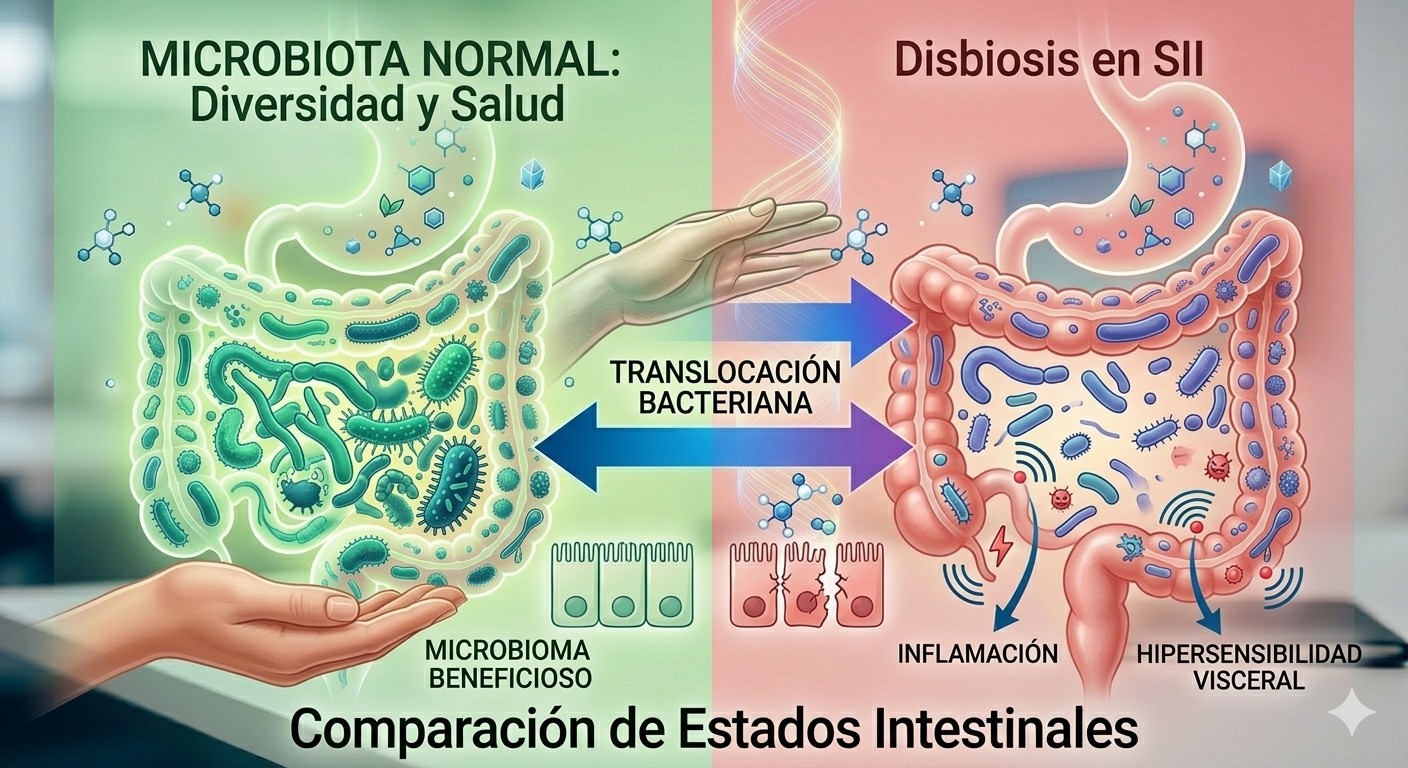
La microbiota intestinal—la comunidad de aproximadamente 100 billones de microorganismos que habita el tracto gastrointestinal—emerge como actor central en la fisiopatología del Síndrome de Intestino Irritable. Décadas de investigación han establecido que alteraciones en esta comunidad microbiana (disbiosis) contribuyen significativamente a síntomas del SII, y que la modulación selectiva de la microbiota mediante probióticos específicos ofrece oportunidad terapéutica validada.
Definiciones clave
Eubiosis: Estado de equilibrio dinámico de la microbiota, con:
- Alta diversidad (>1000 especies diferentes)
- Estabilidad temporal
- Funciones metabólicas intactas
- Capacidad de resistencia ante perturbaciones
Disbiosis: Alteración del balance, composición, o función microbiana, caracterizada por:
- Reducción de diversidad
- Proliferación de organismos potencialmente patógenos
- Pérdida de organismos productores de metabolitos beneficiosos
- Alteración de funciones metabólicas clave
Resiliencia: Capacidad de la microbiota de resistir perturbaciones y retornar al estado basal.
Hallazgos de disbiosis en SII
Múltiples estudios metagenómicos han documentado alteraciones consistentes en SII:
Alteración de proporciones Firmicutes/Bacteroidetes:
- Ratio elevado en algunos estudios (>10:1, versus 1:1 en sanos)
- Asociado con inflamación de bajo grado
- Variable según subtipo (SII-D frecuentemente ratio bajo)
Reducción de Bifidobacterium:
- Presente en ~65-75% de pacientes con SII
- Correlaciona con severidad de síntomas
- Se recupera con tratamiento probiótico exitoso
Alteración de Faecalibacterium prausnitzii:
- Productor de butirato (AGCC anti-inflamatorio)
- Reducido en SII, especialmente SII-D
- Inversamente correlacionado con marcadores inflamatorios
Sobrecrecimiento de potenciales patobiontes:
- Aumento de Proteobacteria (especialmente E. coli, Klebsiella)
- Elevación de Akkermansia muciniphila (paradójicamente, relación compleja)
- Presencia de organismos pro-inflamatorios
Reducción de productores de AGCC:
- Menos capacidad de fermentación de fibra
- Menor producción de butirato, propionato, acetato
- Consecuencias sistémicas y locales (energía de colonocitos)
Mecanismos de daño: de disbiosis a síntomas
1. Alteración de barrera intestinal («Leaky Gut»)
Mecanismo molecular:
- Disbiosis → reducción de productores de butirato
- Menor butirato → debilitamiento de uniones estrechas (tight junctions)
- Debilitamiento de claudinas, occludina, ZO-1
- Aumento de permeabilidad paracelular
Consecuencias:
- Translocación bacteriana (LPS de gram-negativos alcanza lámina propia)
- Activación de TLR-4 en células dendríticas intestinales
- Respuesta innata exagerada
Relevancia en SII:
- Aumento de zonulina (regulador de permeabilidad) en 60% de SII
- Correlaciona con hipersensibilidad visceral
- Reducible mediante restauración de flora butirato-productora
2. Alteración del eje cerebro-intestino
Microbiota produce neurotransmisores:
- GABA (inhibidor): Bifidobacterium, Lactobacillus
- Serotonina (5-HT): Candida, Enterococcus
- Dopamina, norepinefrina: Bacillus, Serratia
Disbiosis → alteración de ratios → síntomas de ansiedad/depresión
Microbiota produce metabolitos bioactivos:
- Ácidos biliares secundarios (modificación de microbiota de ácidos biliares primarios)
- Aryl hydrocarbon receptor (AhR) ligands
- Short-chain fatty acids (SCFA)
Todos estos modulan funciones cerebrales vía nervio vago y circulación sistémica.
3. Respuesta inflamatoria anómala
Inflamación de bajo grado persistente:
- Disbiosis permite mayor translocación de antígenos microbianos
- Mayor exposición a LPS (lipopolisacáridos) de gram-negativos
- Activación de células dendríticas, macrófagos
- Aumento de citoquinas pro-inflamatorias (TNF-α, IL-6, IL-8)
En SII específicamente:
- No es inflamación clínicamente evidente (sin erosiones, úlceras)
- Es «inflamación subclínica» o «low-grade inflammation»
- Detectable en biopsias por aumento de linfocitos intraepiteliales
- Detectable en plasma por elevación leve de PCR/calprotectina
Conexión a síntomas:
- Citoquinas pro-inflamatorias aumentan sensibilidad visceral
- Alteran motilidad muscular
- Estimulan nervios sensoriales
4. Alteración de motilidad intestinal
Microbiota influye en motilidad vía:
- Producción de metabolitos neuroactivos (SCFA, serotonina)
- Efecto directo en células musculares lisas intestinales
- Interacción con sistema nervioso entérico
En disbiosis:
- Alteración de patrón de contracciones
- Fase III del complejo motor migrador anómalo
- Resultado: diarrea (motilidad acelerada) o estreñimiento (retardado)
Rol específico de Bifidobacterium en eubiosis
Características beneficiosas de B. longum:
- Competencia por recursos:
- Fermentación preferencial de fibra indigestible
- Producción de AGCC (especialmente acetato)
- Acidificación luminal (pH < 6) desfavorable para patógenos
- Adhesión epitelial:
- Expresión de adhesinas (proteínas de unión)
- Ocupación de nichos que evita colonización de patógenos
- Fortalecimiento de barrera física
- Producción de antimicrobianos:
- Bacteriocinas naturales contra Clostridium, E. coli
- Reducción competitiva de patobiontes
- Immunomodulación:
- Estímulo de células T regulatorias (Tregs)
- Aumento de IL-10 (anti-inflamatorio)
- Normalización de Th1/Th2
- Aumento de IgA secretoria (defensa mucosal)
- Preservación de barrera:
- Señalización vía PAMPs que refuerza claudinas
- Efecto directo mediante metabolitos (butirato)
Cepa 35624 específicamente:
- Aislada de microbiota de individuo sano
- Optimizada para viabilidad intestinal
- Documentada capacidad de adherencia in vitro
- Eficacia demostrada en restauración de microbiota en estudios metagenómicos
Estudios metagenómicos de cambio de microbiota con probióticos
Hallazgo consistente post-tratamiento con B. longum 35624:
- Aumento de Bifidobacterium (obvio):
- Relativo aumento de 2-10x
- Efecto dosis-dependiente
- Reversible tras discontinuación
- Cambios secundarios (efecto ecológico):
- Aumento de otras Actinobacteria beneficiosas
- Aumento de productoras de butirato (Faecalibacterium)
- Reducción de proteobacterias pro-inflamatorias
- Aumento de Akkermansia muciniphila
- Restauración de función:
- Aumento de genes de fermentación de fibra
- Aumento de genes de síntesis SCFA
- Aumento de genes de homeostasis
- Diversidad:
- Variable; algunos estudios muestran aumento de Shannon index
- Otros muestran estabilización sin cambio numérico
- Probablemente función (genes) > composición (taxonomía)
Alteraciones específicas por subtipo de SII
SII-D (diarrea):
- Disbiosis más severa
- Menor Faecalibacterium
- Mayor Proteobacteria
- Ratio Firmicutes/Bacteroidetes reducido
- Menor producción de SCFA
SII-E (estreñimiento):
- Disbiosis menos severa que SII-D
- Aumento de Firmicutes productoras de gas (Clostridium, Ruminococcus)
- Menor Bacteroidetes
- Alteración de motilidad más que inflamación
SII-M (mixto):
- Disbiosis variable, inestable
- Mayor inflamación que E, menor que D
- Composición dinámica (cambia con síntomas)
SIBO: entidad relacionada pero diferente
Sobrecrecimiento Bacteriano del Intestino Delgado (SIBO):
- Aumento anómalo de bacterias en intestino delgado (<10⁸ CFU/mL normal; >10⁵ en SIBO)
- 60-80% de pacientes con SII-D pueden tener SIBO concurrente
- Tested por breath hydrogen test
Diferencia de disbiosis colónica:
- SIBO es problema de localización (fermentación prematura)
- Disbiosis es problema de composición
- Pueden coexistir
Rol de probióticos en SIBO:
- Paradójicamente, algunos probióticos pueden empeorar SIBO (agregan más bacterias al intestino delgado)
- Tratamiento típico: antibióticos no absorbibles + dieta baja FODMAP
- Probióticos post-tratamiento para restauración
Oportunidades terapéuticas derivadas del entendimiento fisiopatológico
Estrategia 1: Restauración directa (Probióticos)
- Administrar microorganismos beneficiosos específicos
- Alflorex con B. longum 35624: restaura abundancia, función
- Evidencia: mejora de síntomas 60-70%, normalización de inflamación
Estrategia 2: Alimentación selectiva (Prebióticos)
- Sustrato fermentable que selectivamente estimula microorganismos beneficiosos
- Inulina, FOS: estimulan Bifidobacterium
- Combinación Probiótico + Prebiótico (simbiótico) potencialmente superior
- Investigación activa en combinaciones optimales
Estrategia 3: Modulación de permeabilidad
- Glutamina, zinc carnosina: refuerzan tight junctions
- Curcumina: efecto anti-inflamatorio
- Puede complementar a probióticos
Estrategia 4: Dieta como factor modificador
- Dieta baja FODMAP: reduce substrato para fermentación excesiva
- Fibra soluble: estimula productores de butirato
- Combinación dietética + probiótica = máximo efecto
Estrategia 5: Reducción de factores disruptivos
- Evitar antibióticos innecesarios (mayores disruptores)
- Manejo de estrés (estrés altera permeabilidad)
- Evitar irritantes (alcohol, NSAIDs)
Desafío de «sesgo de composición» en investigación
Es importante reconocer que:
- No toda alteración de composición = causa de síntomas
- Algunos cambios metagenómicos son consecuencia, no causa
- Función (genes, metabolitos) probablemente > composición (especies)
- Futuro probablemente incluya metagenómica funcional no solo taxonómica
Perspectiva futura: Biota Engineering
Investigación emergente en manipulación precisa de microbiota:
- Bacteriófagos para eliminar patógenos específicos
- Cápsulas con mezclas microbianas optimizadas
- Metabolitos puros en lugar de bacterias
- Medicina de precisión (terapia según microbiota individual)
Conclusiones clínicas
Entendimiento de microbiota en SII:
- Valida la patología del SII como condición biológica (no puramente psicosomática)
- Justifica intervenciones dirigidas a microbiota (probióticos específicos)
- Explica por qué dieta importa (sustrato para microbiota)
- Predice por qué manejo integral (dieta + estrés + probióticos) es superior a monoabordaje
- Abre futuro de medicina de precisión en SII
Para la práctica clínica: la combinación de B. longum 35624 (restaura eubiosis) + dieta baja FODMAP (reduce substrato patógeno) + manejo del estrés (evita disrupción) = máximo beneficio basado en fisiopatología conocida.
Links internos sugeridos: